Diluição
Consiste em adicionar mais solvente puro a uma determinada solução.
A massa de uma solução após ser diluída permance a mesma, não é alterada, porém a sua concentração e o volume se alteram. Enquanto o volume aumenta, a concentração diminui. Veja a fórmula:
![]()
Onde:
M1 = molaridade da solução 1
M2 = molaridade da solução 2
V1 = volume da solução 1
V2 = volume da solução 2
Para esta fórmula, sempre M1 e V1 são mais concentrados e M2 e V2 são mais diluídos.
Exemplo:
Um químico deseja preparar 1500mL de uma solução 1,4mol/L de ácido clorídrico (HCl), diluindo uma solução 2,8mol/L do mesmo ácido. Qual o volume de solução que havia na primeira solução a ser diluída? Dados:
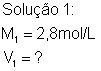

![]()
![]()
![]()
![]()
![]()
Observe que as unidades de volume foram mantidas em mL. Se uma das unidades for diferente, deve-se transformar para litros.