Estequiometria (continuação)
Cálculo de pureza
O cálculo de pureza é feito para determinar a quantidade de impurezas que existem nas substâncias. Estes cálculos são muito utilizados, já que nem todas as substâncias são puras.
Exemplo: uma amostra de calcita, contendo 80% de carbonato de cálcio, sofre decomposição quando submetida a aquecimento, de acordo com a reação:
![]()
Qual massa de óxido de cálcio obtida a partir da queima de 800g de calcita?
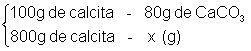
![]()
![]()
x = 640g de CaCO3
Para o restante do cálculo, utiliza-se somente o valor de CaCO3 puro, ou seja, 640g.
![]()
![]()
![]()
![]()
x = 358,4g de CaO
Cálculo de rendimento
É comum, nas reações químicas, a quantidade de produto ser inferior ao valor esperado. Neste caso, o rendimento não foi total. Isto pode acontecer por várias razões, como por exemplo, má qualidade dos aparelhos ou dos reagentes, falta de preparo do operador, etc.
O cálculo de rendimento de uma reação química é feito a partir da quantidade obtida de produto e a quantidade teórica (que deveria ser obtida). Quando não houver referência ao rendimento de reação envolvida, supõe-se que ele tenha sido de 100%. Exemplo:
Num processo de obtenção de ferro a partir do minério hematita (Fe2O3), considere a equação química não-balanceada:
![]()
Utilizando–se 480g do minério e admitindo-se um rendimento de 80% na reação, a quantidade de ferro produzida será de:
Equação balanceada: ![]()
![]()
Dados: 1Fe2O3 = 480g
2Fe = x (m) com 80% de rendimento
MM Fe2O3 = 160g/mol
MM Fe = 56g/mol
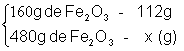
![]()
![]()
x = 336g de Fe
Cálculo de rendimento:
![]()
![]()
![]()
x = 268,8g de Fe